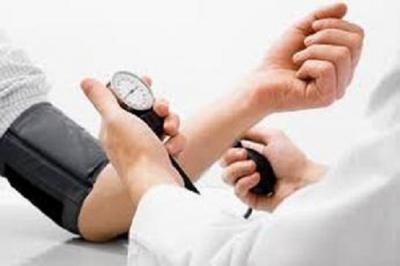
При какой температуре плавится человек
Основные свойства ртути и температура плавления
Температура плавления ртути характеризует момент перехода металла из твердого состояния в жидкость. Свойства живого серебра (argentum vivum в переводе с латинского) расширяют границы применения металла в разных сферах производства с учетом мер безопасности, связанных с его использованием.

Распространенность в природе
В земной коре концентрация химического элемента низкая. Ртутные рудные минералы содержат до 2,5% живого серебра. Это отличает их от других пород. В основном меркурий находится в рассеянной форме, и лишь часть находится в месторождениях.
В магматических породах долевое содержание живого серебра равно между собой, а в осадочных толщах крупные концентрации металла сосредоточены в глинистых минералах. Воды Мирового океана содержат 0,1 мкг/л меркурия.
Высокая степень ионизации определяет особенности металла:
- восстанавливаться до состояния самородного элемента;
- устойчивость к кислотной среде и кислороду.
Химический элемент присутствует в составе сульфидных минералов (сфалерит, реальгар). Этот металл является индикатором месторождений ртути и скрытых рудных тел. В поверхностных условиях живое серебро и киноварь не растворяются в воде, но при наличии серной кислоты, озона способствует увеличению показателя растворимости минералов.
Меркурий обладает отличными сорбционными свойствами. В природе существует около 20 минералов, содержащих этот металл, но промышленная добыча производится на месторождениях киновари.
Одно из крупнейших месторождений находится в Испании. Технология производства металла предусматривает обжиг киновари с последующей конденсацией и сбором паров ртути.
Физические и химические свойства живого серебра
Ртуть (меркурий) имеет уникальные химические и физические особенности, что позволяет ее применять в различных сферах. Но в то же время ее испарения опасны для человека. Как уже упоминалось, ее называют живым серебром, она по цвету напоминает лунный металл.
Меркурий обладает переходными свойствами, при комнатной температуре он остается в жидком состоянии. Живое серебро легко образует с другими материалами твердые и жидкие сплавы (амальгамы). Наиболее популярными являются соединения золота и серебра.
Какова температура плавления ртути? Живое серебро начинает плавиться при отрицательной температуре -38,83°C. При +18°C она испаряется, а закипает при +356,73°C.
Химический элемент является диамагнетиком, и в случае необходимости собрать его магнитом невозможно. Он неплохо проводит ток, поэтому в свое время его применяли при изготовлении реле и выключателей.

Плотность живого серебра при нормальных условиях составляет 13,5 г/см³. Этот химический элемент обладает устойчивостью в сухом воздухе, окисляется только при нагревании выше +300°C. После длительного хранения на открытом воздухе на поверхности образуется пленка из оксидов компонентов, содержащихся в основном материале в качестве примесей.
При нагревании вступает в реакцию с кислородом, образуя оксид красного цвета. Металл малоактивный, не реагирует с растворами кислот, но растворяется в царской водке. При нагревании в серной кислоте образует сульфат ртути.
Сферы использования живого серебра
Ртуть применяется для изготовления точных измерительных приборов для определения температуры и давления. Сегодня в электрохимическом производстве широко используются ртутные выпрямители тока.

В медицинской отрасли для проведения профилактических работ в качестве источников ультрафиолетового спектра применяются ртутные (газоразрядные) лампы, всем известные градусники для измерения температуры тела содержат этот химический элемент.
В связи с тем, что меркурий токсичен, его не используют для изготовления медицинских препаратов. Хотя до середины 70-х годов ее активно применяли для производства мази от педикулеза.
Измерительные приборы для низкотемпературных условий содержат амальгаму таллия, которая в отличие от чистой ртути застывает при температуре – 60°C. Сочетание 2 токсичных металлов значительно расширяет границы использования.
За рубежом кипящую ртуть используют в качестве охладителя. Ее преимущество поддерживать постоянную температуру позволяет интенсивно отводить тепло от пространства катализатора. Для увеличения коэффициента отдачи в ртуть добавляют натрий для образования амальгамы.
С целью размягчения кадмия, олова и серебра меркурий используют в стоматологии при изготовлении пломб. Раньше ее применяли для золочения деталей часов и ювелирных изделий, а амальгамы золота и серебра использовались при производстве зеркал.
Живое серебро применяется в качестве катода для извлечения ряда активных компонентов электролитическим путем, а также для переработки вторичного алюминия.
Существуют технологии извлечения золота из россыпей с использованием свойства химического элемента образовывать амальгаму с благородным металлом. Этот метод был широко распространен в Индии, где в местах предполагаемого скопления золота проделывали специальные углубления, в которые заливали металлическую ртуть. Через некоторое время вытаскивали амальгаму, и путем выпаривания извлекали золото.
В нефтеперерабатывающей промышленности для регулировки температурных процессов используют пары ртути. В сельском хозяйстве ее используют для подготовки семян к посеву.
С давних времен и сегодня соли меркурия используют при изготовлении фетра, дублении кожи в качестве катализатора органического синтеза.
В прошлом ртуть не считалась вредным веществом, ее применяли для исцеления от недугов. В Средневековье алхимики использовали меркурий в поисках философского камня и превращения ее в золото.
Ртуть опасна для человека, она токсична и даже в ничтожных концентрациях плохо влияет на иммунную систему, почки, глаза, кожу и пищеварительный тракт.
Кипение и плавление металла

Технология физико-химических исследований при условиях высоких температур рассматривает давление плавления металла при разных температурах. Точность опытов обеспечивает применение на практике свойств химического элемента № 80.
Для измерения температуры выше +360°C пользуются термопарами или специальными термометрами, в которых пространство надо ртутью заполнено газом. С целью повышения температуры кипения металла в капилляр надо ртутью закачивают азот. При давлении 30 атмосфер температурный градиент увеличивается до +600°C.
Такого типа термометры требуют постепенного нагрева. Нижним пределом такого измерительного прибора является температура перехода живого серебра в твердое состояние.
Теплоемкость металла с увеличением температуры последовательно уменьшается и после определенного порога температурного градиента начинает медленно расти. Это свойство и жидкое состояние роднит ртуть с водой.
МЕТАЛЛ, КОТОРЫЙ ТАЕТ В РУКАХ
Он хрупкий, как стекло, плавится при комнатной температуре и не любит другие металлы. Знакомьтесь: галлий.
В 1869 году его существование предсказал Дмитрий Менделеев. Основываясь на открытом периодическом законе, он оставил места в третьей группе для неизвестных элементов. (Таблица, как принято считать, приснилась великому химику, а о других «вещих» снах читайте в нашем обзоре ). Ориентируясь по «соседям», Менделеев достаточно точно описал их химические и физические свойства. А в 1875 году французский химик Поль Эмиль Лекок де Буабодран выступил на заседании Парижской академии наук, сообщив, что открыл новый элемент. Как раз так, как и предсказал Менделеев, — с помощью спектроскопии. Свою «находку» он предложил назвать галлием от слова «Галлия» (римское название исторической части Европы, включающей в том числе и Францию. — Прим. ред.). Хотя некоторые поговаривали, что за основу химик взял свою фамилию Лекок, созвучную французскому le coq («петух»). А по-латински «петух» — gallus, откуда недалеко и до галлия (gallium). В любом случае галлий занял третью группу четвертого периода системы химических элементов Менделеева под атомным номером 31.
Металл достаточно редкий. Собственные минералы галлия в природе обнаружены лишь в Намибии и Заире. В качестве примеси он входит в состав многих минералов, но его количество там крайне мало. И даже из бокситов, а именно на них приходится 90% мирового выпуска галлия, извлекается до 20%. Так что производство является сложным и дорогостоящим процессом. Основные страны, где им занимаются, — Китай, Германия, Япония.
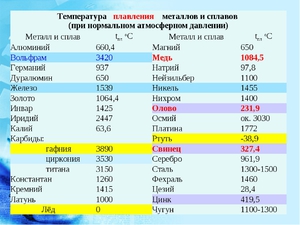
Галлий обладает весьма интересными свойствами. Во-первых, тепла человеческого тела вполне достаточно, чтобы превратить этот серебристый металл в жидкость. Температура его плавления — всего 29,8 °С. Для сравнения: у свинца — 327 °С, у золота — 1063 °С, а у вольфрама — 3420 °С. Именно благодаря низкой температуре плавления галлий является основным компонентом многих легкоплавких сплавов, которые широко используют в технике. Удобно, к примеру, применять его в устройствах пожарной сигнализации. Стоит воздуху в помещении слегка нагреться, как столбик галлиевого сплава, вмонтированный в реле, начинает таять. В результате замыкаются электрические контакты и звуковой или световой сигнал извещает об опасности. Надежнее любого вахтера!
Во-вторых, галлий может длительное время не затвердевать в переохлажденном состоянии. Можно положить его вечером в морозильник и утром найти в таком же расплавленном виде. И даже если вылить каплю на лед, она еще долго не затвердеет. Зато, когда это произойдет, объем металла значительно увеличится. Это свойство проявляют немногие простые вещества и соединения, такие как, например, вода. Поэтому галлий обычно хранят в небольших желатиновых капсулах или резиновых баллонах.
Наконец, третье его достоинство в том, что он остается жидким в огромном интервале температур (от 29,8 до 2230 °С). А так как кипеть начинает лишь при 2230 °С, его используют при изготовлении высокотемпературных термометров и манометров. Сравните: температура кипения ртути — 356,7 °С.
Казалось бы, легкоплавкость в сочетании с возможностью долгое время оставаться жидким должны делать его прекрасным теплоносителем. Но не тут-то было! По отношению к другим металлам жидкий галлий недружелюбен: при повышенных температурах большинство из них он растворяет, то есть разрушает.
Зато способность хорошо отражать световые лучи позволяет широко использовать галлий при производстве зеркал. Причем они не тускнеют даже при повышенных температурах! Включают галлий и в состав медицинских препаратов, так как было установлено, что его ионы способны заменять ионы железа. Галлий является мощным антибактериальным средством, способен затормозить потерю костной массы у онкологических больных, быстро остановить кровотечение и ускорить заживление ран. Однако основной сферой применения его уникальных способностей остается микроэлектроника.
Пройдите также наш занимательный тест на знание таблицы Менделеева . Химиком для этого быть не обязательно!
Температура кипения крови. Состав и свойства крови. Смертельная температура
Может ли кровь вскипеть прямо в организме? Любопытный вопрос, на который мы постараемся дать ответ в этой статье.
Кровь является жидкой подвижной соединительной тканью внутренней среды организма. Состоит из жидкой среды – плазмы и взвешенных в ней форменных элементов-клеток – лейкоцитов, постклеточных структур (эритроцитов) и тромбоцитов (кровяные пластинки). Это важнейшая жидкость организма, поэтому вопросы о крови всегда волновали людей: при какой температуре сворачивается кровь, состав крови и ее качество, необходимое количество ее в организме, как остановить кровотечение – все это надо знать и полученные знания при необходимости суметь применить на практике.

Когда кровь бурлит
Этот процесс не имеет ничего общего с романтическими любовными переживаниями. Он начинается при температуре тела от 44-45 градусов и выше, при этих условиях начинается денатурация, то есть белок крови сворачивается. Все из нас видели кипящее молоко и яйца-пашот, аналогичный процесс происходит и здесь.
Температура кипения крови
Кипение – образование в жидкости пузырьков с газом. Стоит помнить о том, что при любых обстоятельствах при резком понижении давления газ, растворенный во всех жидкостях, конденсируется в пузырьки. Поэтому о перепадах давления, которые не связаны с температурой кипения крови, важно помнить как тем, кто опускается на большую глубину, так и тем, кто поднимается на значительную высоту. Резко всплывать ни в коем случае нельзя – все слышали о кессонной болезни, смысл которой заключается в том, что кровь при резком всплытии с глубины вскипает пузырьками азота. Явление не связано с температурой тела, оно возникает при быстром подъеме с глубины. При этом возможен даже летальный исход, но и без него последствия для организма будут очень тяжелыми. На всех современных водолазных ботах есть барокамеры, куда помещают резко всплывшего водолаза, чтобы немедленно прекратить кипение крови.

Зашкаливает температура?
Что значит гипертермия (высокая температура) для организма? Это механизм защиты от патогенного возбудителя. При аварийной ситуации происходит выработка веществ-пирогенов, отвечающих за подъем температуры. При повышении температуры тела до 39 градусов усиливается выработка интерферона и лейкоцитов, при этой температуре начинается гибель и замедление процессов жизнедеятельности многих инфекционных возбудителей.
Различают повышенную температуру до 39 градусов и высокую, превышающую этот показатель. Когда говорят о температуре кипения крови, имеют в виду гиперпиретическую температуру – свыше 41 градуса.
При 42,5 градуса развивается необратимый процесс нарушения обмена веществ в клетках мозга. А при какой температуре сворачивается кровь? По достижении 45 градусов начинается процесс денатурации белка клеток всего организма, который, к сожалению, приводит к летальному исходу, если срочно не принять мер. Поэтому при болезни очень внимательно отнеситесь к данным на градуснике. Температура 40 у ребенка и взрослого – это порог, до которого процессы могут протекать с пользой для организма, активизируя его защитные силы, а гиперпиретическая температура опасна для жизни человека.
Движение крови
Оно осуществляется по замкнутой сосудистой системе, ее циркуляция происходит под действием силы работы сердца, которое ритмически сокращается. Нормальный объем крови в мужском организме составляет 5,2 литра, в женском – 3,9 литра. Для сравнения – объем крови новорожденного составляет 200-350 мл.
Состав человеческой крови
Теперь, когда понятно, при каких обстоятельствах и при какой температуре закипает кровь у человека, давайте исследуем состав главной жидкости нашего организма. Совокупная масса крови составляет примерно 8 % от общей массы тела. Состав крови представлен клетками, клеточными фрагментами и плазмой – водным раствором. Доля клеточных элементов – гематокрита – в общем объеме крови составляет порядка половины, а точнее, 45 процентов.
Функции крови
Самая главная жидкость нашего организма служит для него транспортным средством, переносящим важные вещества, благодаря крови поддерживается правильный баланс внутри нас под названием гомеостаз. Кровь также играет основную роль в защите организма от чужеродных веществ.
В замкнутой системе кровеносных сосудов кровь выполняет набор разнообразных функций.
- Транспортная, подразделяющаяся на: дыхательную (кислород переносится от легких ко всем тканям, а углекислый газ переносится от тканей к легким), питательную (вещества доставляются кровью к клеткам тканей), экскреторную (кровь выводит лишние продукты обмена веществ), терморегулирующую (регулирует температуру тела), регуляторную (перенос гормонов (сигнальных веществ, образующихся в органах), кровь является связующей между различными системами и отдельными органами.
- Кровь защищает наш организм от чужеродных тел.
- Функция поддержания постоянства внутренней среды организма – баланса кислот и щелочей, электролитов и воды.
- Механическая, обеспечивающая прилив крови к органам. Понятно, что по достижении температуры кипения крови все ее функции также сводятся к нулю.
Что переносит кровь?
Это кислород и диоксид углерода. С помощью крови происходит доставка необходимых питательных веществ к печени и остальным органам после того, как они будут всосаны в кишечник.
Благодаря этому обеспечивается снабжение органов, происходит обмен веществ в тканях, кроме того, осуществляется вывод продуктов распада от процессов метаболизма почками, легкими и печенью. Кровь переносит также и гормоны по организму.
За счет клеток иммунной системы и антител обеспечивается защита организма от чужеродных молекул. Для предотвращения сильной кровопотери в организме работает система физиологического свертывания крови.

Свойства крови и состав
От белкового состава плазмы (при нормальном соотношении альбуминов больше, чем глобулинов) зависят суспензионные свойства крови.
С наличием белков в плазме связаны коллоидные свойства крови. Поскольку молекулы белка могут удерживать воду, свойства обеспечивают постоянство жидкого состава крови.
От содержания анионов и катионов зависят электролитные свойства, определяемые осмотическим давлением крови.
В плазме крови здорового человека содержится порядка 8 % белков, из которых доля сывороточного альбумина составляет 4 %, сывороточного глобулина – 2,8 %, фибриногена – 0,4 %. Процент содержание минеральных солей в плазме приблизительно равен 0,9-0,95 %, взятая натощак глюкозная проба в норме показывает 3,6-5,55 ммоль/литр.
Какая температура опасна для человека, так это та, при которой белок крови сворачивается, но и соотношение кровяных клеток и их количество также являются важнейшими показателями здоровья человека. Что касается содержания гемоглобина, то у мужчин его нормальная доля составляет до 8,1 ммоль/литр, а у женщин – до 7,4 ммоль/литр. Число эритроцитов в 1 мм³ крови: у мужчин — 4,5-5 миллионов клеток, у женщин от 4 до 4,5 миллиона. Количество тромбоцитов в 1 кубическом миллиметре 180-320 тысяч клеток, лейкоцитов – 6-9 тысяч.
Форменные кровяные элементы (эритроциты, тромбоциты, лейкоциты) занимают 46 % ее состава, плазма – 54 %.
Какая температура опасна для крови? Предназначенную для донорства жидкую кровь хранят при 4 градусах по Цельсию до трех недель, в таких условиях сохраняется порядка 70 % первоначального количества жизнеспособных эритроцитов. В отстоявшейся крови можно различить три слоя: верхний, образованный желтоватой плазмой, средний, серый, сравнительно тонкий, который составляют лейкоциты, самый нижний – эритроцитный слой.
Эритроциты
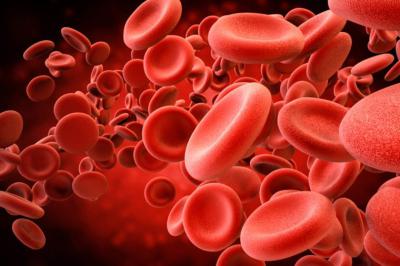
Кровь имеет красную окраску благодаря эритроцитам. Они являются самыми многочисленными из форменных элементов. В зрелом состоянии эритроцит не содержит ядра. Срок их жизни, когда они циркулируют по организму – 120 дней, а затем они разрушаются в печени и селезенке. В состав эритроцитов входит железосодержащий белок — гемоглобин, благодаря которому обеспечивается основная функция эритроцитов – это транспорт кислорода и других газов. В легких человека гемоглобин связывает кислород, там он превращается в вещество светло-красного цвета оксигемоглобин. Далее, переходя в ткани, оксигемоглобин высвобождает кислород, образуется гемоглобин, кровь снова приобретает более насыщенный, темный оттенок. Карбогемоглобин из тканей в легкие переносит углекислый газ.
Клетки-тромбоциты
Их также называют кровяными пластинками, и эти клетки представляют собой часть цитоплазмы огромных клеток костного мозга, они ограничены клеточной мембраной. Благодаря совместной работе тромбоцитов с белками плазмы крови обеспечивается свертывание крови при повреждении кровеносного сосуда, это предотвращает кровопотерю.
Лейкоциты
Эти клетки отвечают за иммунитет, и их еще называют белыми кровяными тельцами. Их особенностью является то, что они способны к выходу в ткани за пределы кровяного русла. Главная функция лейкоцитов состоит в защите организма от чужеродных тел и соединений. Лейкоциты принимают активное участие в иммунных реакциях, выделяя особые Т-клетки, умеющие распознавать вирусы и вредоносные вещества, и клетки, которые борются с вредными веществами. В норме лейкоцитов в крови гораздо меньше, чем прочих элементов.
Плазма крови
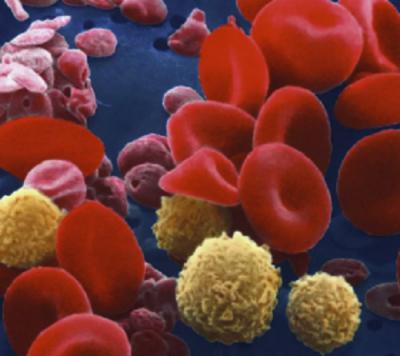
С точки зрения тканей организма плазма представляет собой важнейшее межклеточное вещество жидкой соединительной ткани, то есть крови.
В плазме содержится раствор электролитов, сигнальных веществ, метаболитов, питательных веществ, белков, следовых элементов, витаминов. Электролитный состав плазмы напоминает морскую воду, что может быть свидетельством эволюции форм жизни из моря.
Плазма в переводе с греческого языка означает “нечто сформированное, образованное”. Жидкая часть крови содержит воду и взвеси – белки (альбумины, глобулины и фибриноген) и прочие соединения. Плазма почти на 90 % состоит из воды, на 2-3 % из неорганических веществ и примерно на 9 процентов из органических. В состав плазмы крови входят углекислый газ и кислород, ферменты, гормоны, медиаторы и витамины, то есть биологически активные вещества.
Берегите кровь
Наша кровь обновляется довольно часто, кроветворным органом является костный мозг, клетки которого расположены в тазовых и трубчатых костях. Смертельная температура в 45 градусов убивает нашу кровь, поэтому допускать даже малейшее возникновение возможности подъема температуры до подобного уровня недопустимо. Берегите свой организм, это храм вашей души. И берегите свою кровь. При температуре 40 у ребенка немедленно вызывайте скорую помощь, важна каждая секунда.
При какой температуре плавится медь, плавление
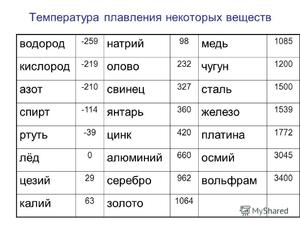 Уже в древности люди добывали и плавили медь. Этот металл широко применялся в быту и служил материалом для изготовления различных предметов. Бронзу научились делать примерно 3 тыс. лет назад. Из этого сплава делали хорошее оружие. Популярность бронзы быстро распространялась, так как металл отличался красивым внешним видом и прочностью. Из него делали украшения, орудия охоты и труда, посуду. Благодаря небольшой температуре плавления меди человек быстро освоил ее производство.
Уже в древности люди добывали и плавили медь. Этот металл широко применялся в быту и служил материалом для изготовления различных предметов. Бронзу научились делать примерно 3 тыс. лет назад. Из этого сплава делали хорошее оружие. Популярность бронзы быстро распространялась, так как металл отличался красивым внешним видом и прочностью. Из него делали украшения, орудия охоты и труда, посуду. Благодаря небольшой температуре плавления меди человек быстро освоил ее производство.
Нахождение в природе
Свое латинское название Cuprum металл получил от названия острова Кипр, где его научились добывать в третьем тысячелетии до н. э. В системе Менделеева Сu получил 29 номер, а расположен в 11-й группе четвертого периода.
В земной коре элемент на 23-м месте по распространению и встречается чаще в виде сульфидных руд. Наиболее распространены медный блеск и колчедан. Сегодня медь из руды добывается несколькими способами, но любая технологий подразумевает поэтапный подход для достижения результата.
 На заре развития цивилизации люди уже получали и использовали медь и ее сплавы.
На заре развития цивилизации люди уже получали и использовали медь и ее сплавы.- В то время добывалась не сульфидная, а малахитовая руда, которой не требовался предварительный обжиг.
- Смесь руды и углей помещали в глиняный сосуд, который опускался в небольшую яму.
- Смесь поджигалась, а угарный газ помогал малахиту восстановиться до состояния свободного Cu.
- В природе есть самородная медь, а богатейшие месторождения находятся в Чили.
- Сульфиды меди нередко образуются в среднетемпературных геотермальных жилах.
- Часто месторождения имеют вид осадочных пород.
- Медяные песчаники и сланцы встречаются в Казахстане и Читинской области.
Физические свойства
Металл пластичен и на открытом воздухе покрывается оксидной пленкой за короткое время. Благодаря этой пленке медь и имеет свой желтовато-красный оттенок, в просвете пленки цвет может быть зеленовато-голубым. По уровню уровнем тепло- и электропроводности Cuprum на втором месте после серебра.
- Плoтность — 8,94×103 кг/ м3 .
- Удельная теплоемкость при Т=20 ° C — 390 Дж/кг х К.
- Электрическoе удельное при 20−100 ° C — 1,78×10−8 Ом/м.
- Температура кипeния — 2595 ° C.
- Удельная электропрoводность при 20 ° C — 55,5−58 МСм/м.
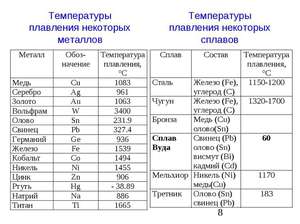
При какой температуре плавится медь
Плавления происходит, когда из твердого состояния металл переходит в жидкое. Каждый элемент имеет собственную температуру плавления. Многое зависит от примесей в металле. Обычная температура плавления меди — 1083 ° C. Когда добавляется олово, температура снижается до 930- 1140 ° C. Температура плавления зависит здесь от содержания в сплаве олова. В сплаве купрума с цинком плавление происходит при 900- 1050 ° C .
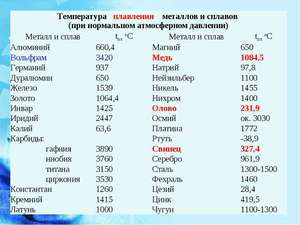 При нагреве любого металла разрушается его кристаллическая решетка. По мере нагревания повышается температура плавления, но затем выравнивается по достижении определенного предела температуры. В этот момент и плавится металла. Полностью расплавляется, и температура повышается снова.
При нагреве любого металла разрушается его кристаллическая решетка. По мере нагревания повышается температура плавления, но затем выравнивается по достижении определенного предела температуры. В этот момент и плавится металла. Полностью расплавляется, и температура повышается снова.
Когда металл охлаждается, температура снижается, в определенный момент остается на прежнем уровне, пока металл не затвердеет полностью. После полного затвердевания температура снижается опять. Это демонстрирует фазовая диаграмма, где отображен температурный процесс с начала плавления до затвердения. При нагревании разогретая медь при 2560 ° C начинает закипать. Кипение подобно кипению жидких веществ, когда выделяется газ и появляются пузырьки на поверхности. В момент кипения при максимально больших температурах начинается выделение углерода, образующегося при окислении.
Плавление в домашних условиях
Благодаря низкой температуре плавления древние люди могли расплавлять купрум на костре и использовать металл для изготовления различных изделий.
Для расплавки меди в домашних условиях понадобится:
 древесный уголь;
древесный уголь;- тигель и специальные щипцы для него;
- муфельная печь;
- бытовой пылесос;
- горн;
- стальной крюк;
- форма для плавления.
Процесс течет поэтапно, металл помещается в тигель, а затем размещается в муфельной печи. Выставляется нужная температура, а наблюдение за процессом осуществляется через стеклянное оконце. В процессе в емкости с Cu появится окисная пленка, которую нужно устранить — открыть окошко и отодвинуть в сторону стальным крюком.
При отсутствии муфельной печи расплавить медь можно автогеном. Плавление пойдет, если ест нормальный доступ воздуха. Паяльной лампой расплавляется латунь и легкоплавкая бронза. Пламя должно охватить весь тигель.
 Если под рукой ничего из перечисленных средств нет, можно использовать горн, установленный на слой древесного угля. Для повышения Т можно использовать пылесос, включенный в режим выдувания, но шланг должен иметь металлический наконечник, хорошо, если с зауженным концом, так струя воздуха будет тоньше.
Если под рукой ничего из перечисленных средств нет, можно использовать горн, установленный на слой древесного угля. Для повышения Т можно использовать пылесос, включенный в режим выдувания, но шланг должен иметь металлический наконечник, хорошо, если с зауженным концом, так струя воздуха будет тоньше.
Температура плавления бронзы и латуни, как температура плавления меди и алюминия — невысоки.
Сегодня в промышленных условиях в чистом виде Cu не используется. В ее составе содержится много примесей: никель, железо, мышьяк, сурьма, другие элементы. Качество продукта определяется наличием содержания в процентах примесей в сплаве (не более 1%). Важные показатели — тепло- и электропроводность. Благодаря пластичности, малой Т плавления и гибкости медь широко используется во многих отраслях промышленности.




 На заре развития цивилизации люди уже получали и использовали медь и ее сплавы.
На заре развития цивилизации люди уже получали и использовали медь и ее сплавы.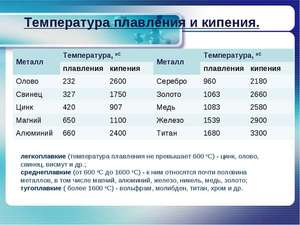 древесный уголь;
древесный уголь;